Брошенный в воду кусочек сахара через некоторое время исчезает – становится невидимым. Мы говорим: «Сахар растворился». Нальем в блюдце несколько капель одеколона. Очень скоро блюдце снова станет сухим. Мы говорим: «Одеколон испарился». Но что означают эти привычные слова?
Сладкий вкус воды и запах, распространившийся но всей комнате, ясно говорят, что ни сахар, ни душистые вещества одеколона не исчезли. Что же случилось с растворившимся сахаром и испарившимся одеколоном?
Подобные вопросы возникли перед людьми, как только они научились размышлять над происходящими вокруг них явлениями природы. Что происходит с жидкостью, когда она испаряется? Почему твердые вещества при нагревании обращаются в жидкости, а при охлаждении снова затвердевают? Как объяснить, что при нагревании тела расширяются, увеличиваются в объеме? Все это требовало ответа, занимало пытливый ум человека. И уже много тысячелетий назад зародилась мысль о том, что все вещества состоят из мельчайших и потому невидимых частиц.
Растворяясь, вещество распадается на невидимые частицы, которые смешиваются с такими же невидимыми частицами воды. Частицы жидкости отрываются от ее поверхности и улетают, рассеиваясь в окружающем пространстве – жидкость испаряется. То же происходит со всякой испаряющейся жидкостью.
У твердых веществ частицы прочно соединены между собой, но под действием теплоты связь между ними ослабевает и твердое вещество превращается в жидкость. Тела при нагревании расширяются потому, что увеличивается расстояние между невидимыми частицами, из которых они состоят. Предположение о таком «зернистом» строении веществ позволяло объяснить очень многие и очень разные явления.
Сначала это было только смелой догадкой. Наука в те далекие времена была еще в младенческом возрасте и не могла ни доказать существования невидимых частиц, ни исследовать их. Но прошли века, и догадка превратилась в строго обоснованную научную теорию. Сейчас учение о невидимых частицах лежит в основе всех наук о веществе. Ученые нашли совершенно бесспорные доказательства существования этих частиц и разработали остроумные, точные и надежные способы их изучения.
Итак, брошенный в воду сахар распадается на невидимые частицы. Эти частицы называются молекулами. Молекулы очень малы. Измерять их привычными мерами длины – сантиметрами или миллиметрами – это все равно, что измерять толщину волоса километрами. В мире невидимых частиц приняты свои единицы измерения. Называется эта мера длины ангстрем (по имени ученого, применившего ее) и обозначается А. Она равна стомиллионной доле сантиметра.
Число молекул даже в крохотной пылинке вещества огромно. Вообразите, что вы бросили одну единственную крупинку сахарного песка в Байкал. Если теперь хорошенько «размешать» озеро, чтобы молекулы сахара равномерно распределились по всему его объему, то в каждом литре байкальской воды окажется свыше двухсот молекул сахара. А если бы молекулы, из которых состоит тот же крошечный кристаллик, можно было бы поровну раздать всем живущим на земле людям, то каждому досталось бы по два миллиарда молекул.
Почему свойства веществ различны?
Мы знаем очень много разных веществ: соль, мел, сахар, воду, медь, железо, спирт, уксус и так далее. Различаем эти вещества по внешнему виду, вкусу, запаху и другим характерным признакам, свойствам. Возникает вопрос: почему свойства веществ различны? Почему, например, спирт легко воспламеняется, а вода не горюча? Почему сахар обугливается при нагревании, а соль – нет?
Если бы мы могли рассматривать молекулы увеличенными в десятки миллионов раз, то увидели бы, что молекулы, как они ни малы, построены, в свою очередь, из еще меньших частиц – атомов. Атомы, составляющие молекулу, тесно соединены между собой и расположены в определенном порядке.
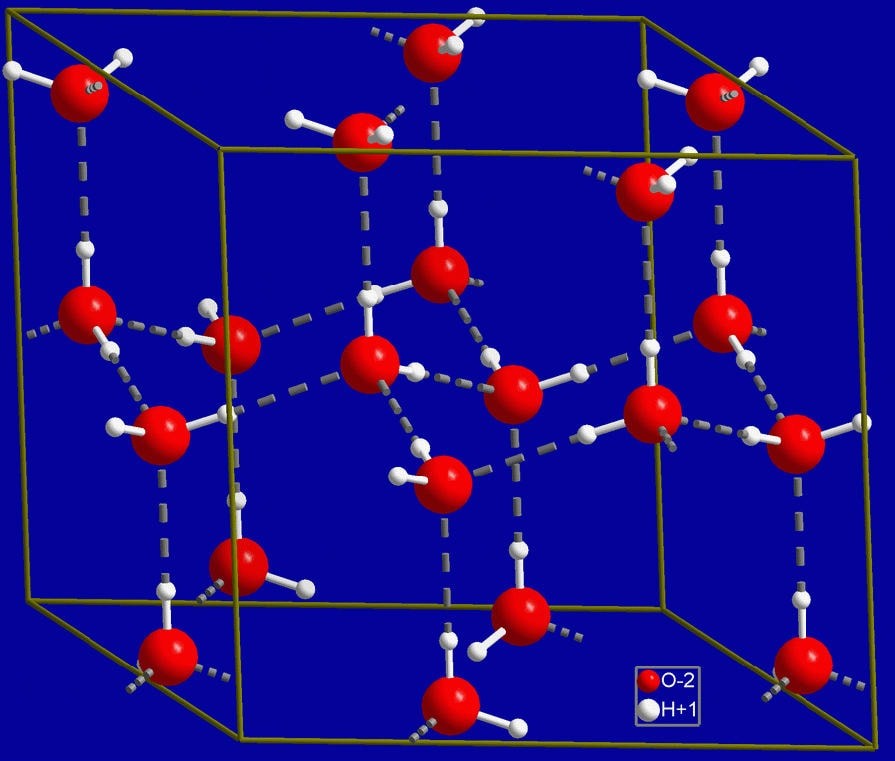
Сравните молекулу воды с молекулой сахара
Молекула воды состоит всего из трех атомов, а в очень сложной молекуле сахара их гораздо больше, различны размеры этих молекул, их вес, взаимное расположение атомов в них. В этом и кроется причина различия между веществами; их свойства различны потому, что каждое вещество состоит из иных молекул, чем все остальные вещества. И только до тех пор, пока молекулы вещества остаются неизменными, пока не меняется их строение, вещество остается самим собой.
Растворяя сахар, мы раздробляем его на отдельные молекулы, но не разрушаем, не повреждаем самих молекул, и сахар остается сахаром, сохраняет свои свойства (например, сладкий вкус). Ну, а если пойти дальше и раздробить молекулы? Что тогда станет с сахаром?
Что же, это можно сделать!
Для этого достаточно нагреть сахар. Он расплавится, потемнеет, из него будут выделяться неприятно пахнущие газы, и вскоре от сахара останется только немного легкого пористого угля. Под действием высокой температуры молекулы сахара распадаются, и сахар превращается в несколько других веществ, свойства которых совсем не похожи на свойства сахара. Одни из них улетают в виде паров и газов, другие остаются в виде углистого остатка. Разрушение молекул привело к разрушению сахара, к превращению его в другие вещества.
Молекулы – это не просто ничтожно малые крупинки или капельки вещества, отличающиеся от больших кусков и капель только размерами. Между самой маленькой крупинкой вещества, состоящей всего из нескольких молекул, и молекулой есть существенное различие: крупинку можно разделить на части, не разрушая самого вещества, с молекулой этого сделать нельзя.





